Aprende Quimica
viernes, 18 de octubre de 2019
viernes, 2 de agosto de 2019
lunes, 25 de febrero de 2019
Semana 6
Formas Alotrópicas
Grafito:
Esta es una forma mas comunes del carbono, este posee una estructura laminar que se encuentran separadas por capas, la fuerza entre ellas es débil, esto hace que el grafito sea blando.
Diamante:
Esta una forma del carbono muy conocida, que se caracteriza por su alto nivel de dureza y por su alta dispersión de luz, tiene una estructura de cristal covalente tridimensional, que se encuentra formados por enlaces de carbono interconectados, que se extienden por todo el cristal.
Fullereno:
Se forma cuando el grafito se vaporiza con un láser, esta forma permite que el carbono pueda combinarse formando hexágonos y pentágonos y estructuras tridimensionales cerradas, se presenta en formas esféricas; el mas común de los fullerenos es el de C60 (de sesenta átomos de carbono).
El Nanotubo de carbón
Es otra forma alotrópica del carbón, su estructura se puede considerar como grafito enrollado en forma de tubo, pueden ser abiertos o cerrados.
La Nanoespuma.
Es otra forma alotrópica del carbono descuebierta en 1997; consiste en un ensamblado de cúmulos de baja densidad de átomos de carbono, mantenidos en una red tridimensional.
Esta es la estructura propuesta para la nanoespuma de carbón.
Ciclo del carbono
Es un ciclo por el cual el carbono se intercambia entre la biosfera, la litosfera, la hidrosfera y la atmósfera de la Tierra. En el planeta Tierra, el carbono circula a través de los océanos, de la atmósfera y de la superficie y el interior terrestre, en un gran ciclo biogeoquímico.

Semana 5
Teoría de Hibridación

La teoría de hibridación de orbitales, establecida por Linus Pauling en su obra publicada en 1931 The Nature of the Chemical Bond, complementa la teoría de enlace de valencia a la hora de explicar la formación de enlaces covalentes. En concreto, la hibridación es el mecanismo que justifica la distribución espacial de los pares de electrones de valencia (lineales, triangulares planas y tetraédricas). Los tipos de hibridación de orbitales que necesitamos aplicar para justificar la geometría de las moléculas más simples son: sp, sp2 y sp3.
Las ideas básicas que permiten una primera aproximación al modelo de hibridación son:
- Un orbital híbrido es una combinación de orbitales atómicos
- El número de orbitales híbridos que se forman es igual al número de orbitales atómicos que se combinan.
- Los orbitales híbridos formados tienen la misma forma y una determinada orientación espacial: sp lineal; sp2 triangular plana y sp3 tetraédrica.
- Los orbitales híbridos disponen de una zona o lóbulo enlazante y otra zona o lóbulo antienlazante; el enlace se produce por el solapamiento del lóbulo enlazante con el otro orbital del átomo a enlazar.

lunes, 11 de febrero de 2019
Semana 4
Realizamos laboratorio sobre las leyes de los gases
Materiales:
Materiales:
- 3 bombas medianas
- 2 bombas grandes
- manguera de venoclisis
- 2 jeringas
- bicarbonato
- pincho delgado
- vela
- fosfoos
Logros
Demostrar experimentalmente la ley de los gases,
lunes, 4 de febrero de 2019
Semana 3
Leyes de los gases
Condiciones normales o ideales de un gas:


- Ley de Boyle-Mariotte
- Ley de Charles
- Ley combinada de los gases o de Avogadro
- Ley de los gases idales
- Ley de Daltón o presiones parciales
Condiciones normales o ideales de un gas:
- Temperatura a 273°K
- Presion a 1atm
- Volumen a 22,4L
- Cantidaad igual a 1mol
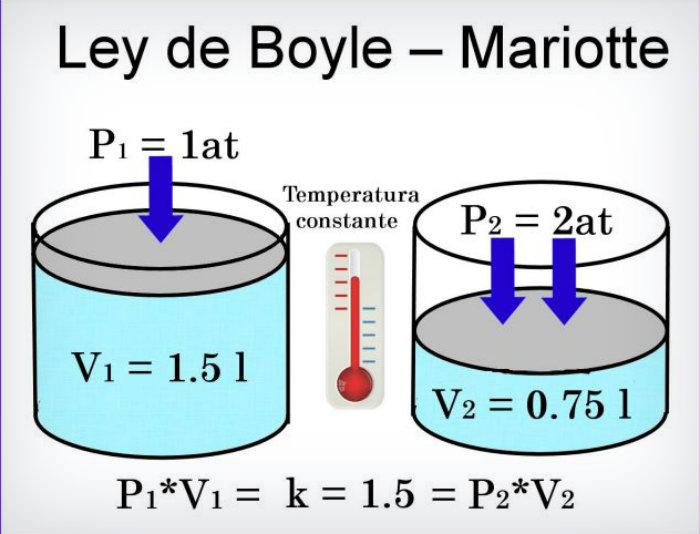
Ley de Boyle

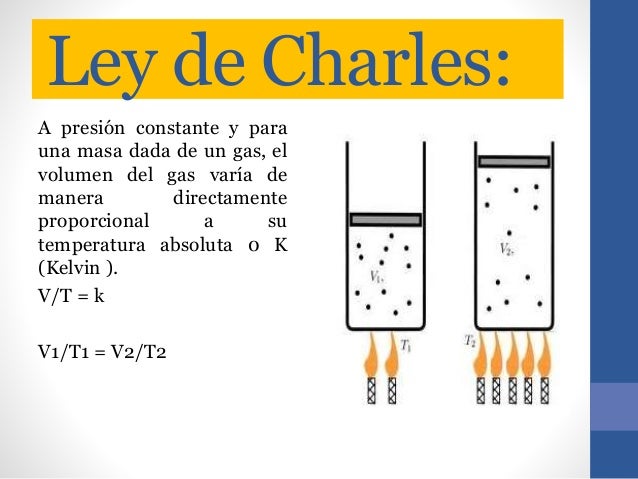
Ley de Charles

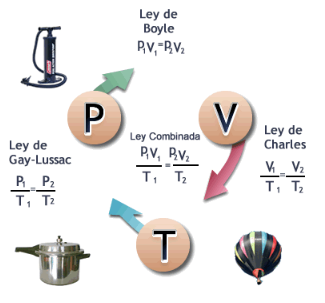
Ley combianda de los gases:
A medida que agregamos gas a un globo, éste se expande, por lo tanto el volumen de un gas depende no sólo de la presión y la temperatura, sino también de la cantidad de gas. Establece que el volumen de un gas mantenido a temperatura y presión constantes, es directamente proporcional al número de moles del gas presentes:

Ley de Daltón
La presion de un gas es igual a la suma de las presiones de los gases parciales que la componen. P1 + P2 + P3... Pn = PT
La presion de un gas es igual a la suma de las presiones de los gases parciales que la componen. P1 + P2 + P3... Pn = PT

Ley de Avogadro

lunes, 28 de enero de 2019
Suscribirse a:
Comentarios (Atom)





